Гликирование и коллаген остров адекватности в океане мракобесия
- Автор: Команда YOUR.OWN
- 2022-10-03
Среднее время прочтения: 12 минут
Сложность темы: средняя
Когда мы говорим о коллагене в коже, то нам нужно разобраться и в двигателе, и в колесах и в корпусе, учесть подушки безопасности и вообще посмотреть на адекватность того, кто у руля. Это настолько популяризированная тема, насколько изучаемо-неизученная, что ей будет посвящена данная статья с разбором имеющихся доказательств и пробелов научных знаний.
Скорость нормального старения пока не удается замедлить, однако предупредить ускоренное старение, вероятно, можно.
Люди одного и того же возраста могут выглядеть по-разному. Одна из ключевых причин старения кроется во внеклеточном матриксе, окружающем наши клетки и формирующем наши ткани, в частности, если мы говорим о коже. Наиболее значимым виновником ключевых причин является гликозилирование, а точнее - глюкосепановые сшивки белка-коллагена.
Есть факты, которые важны, чтобы не поддаваться на уловки маркетинга:
- Глюкосепан разрушить нельзя;
- Первичные продукты гликирования можно разрушать или уменьшать степень и скорость их образования. (рисунок 1)
К первичным продуктам гликирования относятся: продукты Амадори (например, фруктозамин), и основания Шиффа. Давайте рассмотрим механизмы их образования и как супплементарная поддержка организма, образ жизни и питания могут повлиять на сокращение интенсивности преждевременного старения за счет дисфункции коллагенового каркаса кожи.
Существует необходимость разработки разрушителей основного КПГ (конечных продуктов гликирования) во внеклеточном матриксе — глюкосепана. Это должна быть небольшая молекула или фермент, способная проникать между фибриллами коллагена и достигать своей цели — сшивок КПГ. Создание в этом году командой Дэвида Шпигеля антитела [9], нацеленного на глюкоcепан, также добавляет нам шансов в борьбе со старением матрикса дермы.
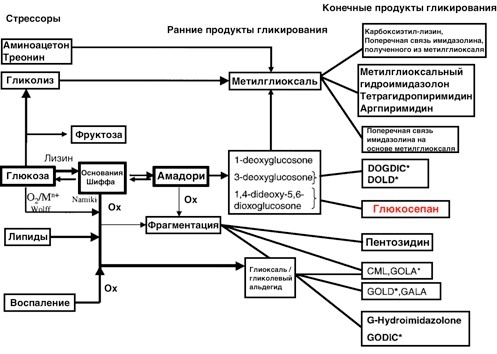
Рисунок 1. На пути формирования глюкосепана сначала образуются основания Шиффа [1]
Гликирование — это присоединение различных сахаров к аминогруппам белков.
Есть определенная норма (ферментативного) присоединения к белкам сахаров - гликозилирование. Это важный, а главное, физиологический процесс отвечающий за нормальное функционирование белка.
Но есть и не норма - неферментативное присоединение сахаров к белкам, оно связано с развитием патологий, нарушением межклеточной коммуникации, с истощением стволовых клеток, клеточным старением, геномной нестабильностью, дисфункцией митохондрий, нарушением целостности барьеров (кишечного и гематоэнцефалического), сердечно-сосудистыми и нейродегенеративными патологиями и, конечно, преждевременным старением [6]. Неферментативное гликирование бывает двух типов, в зависимости от источника:
- Эндогенное (то есть формирующееся по внутренним причинам);
- Экзогенное (по внешним причинам).
Эти процессы объясняет параметаболическая теория старения, или делетериома. Такие процессы старения тесно связаны [7] с побочными реакциями нормального метаболизма, которые мы обсудили выше.
- Эндогенное гликирование — это достаточно медленный, но постоянный процесс, в ходе которого образуются белковые сшивки долгоживущих белков (коллагена, эластина). И оно усиливается в процессе старения, коррелируя исключительно со временем.
- Экзогенное гликирование происходит под воздействием внешних факторов: пищи, приготовленной при высоких температурах и/или с высоким гликемическим индексом, сигаретного дыма, воздуха, загрязненного продуктами горения и др. Повышенный уровень глюкозы в крови, воспаление и окислительный стресс ускоряют процессы гликирования.
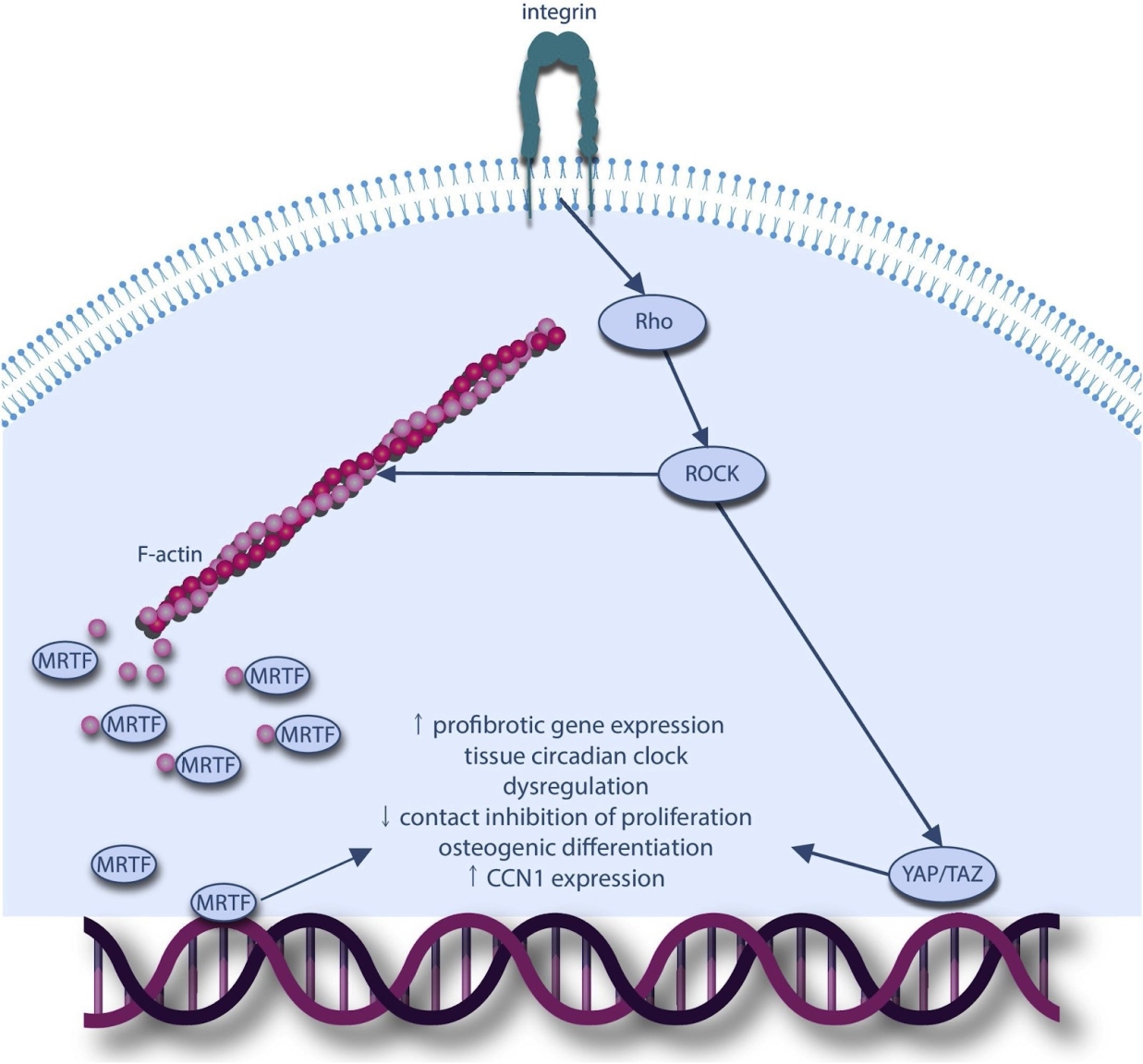
Рис. 2. Жесткий внеклеточный матрикс через интегрины активирует Rho-ROCK и нижестоящие цели: MRTF и YAP / TAZ. Что, в свою очередь, индуцирует экспрессию профибротических генов, дисрегуляцию тканевых циркадных часов, остеогенную дифференцировку, подавляет контактное ингибирование пролиферации и, возможно, индуцирует клеточное старение через активацию CCN1 [6].
Согласно параметаболической теории: биологические молекулы и все биологические процессы несовершенны. Всегда возникают повреждения, и их так много, что неделящиеся клетки не могут с ними справиться. И это независимо от того, как эволюция сформировала организм. Более того, защитные функции от этого повреждения сами по себе будут несовершенными и вызовут другие формы повреждений.
Это можно описать как “ошибки повреждения”. Большинство этих форм повреждений будут просто невидимы для эволюционных процессов, поскольку отбор никогда не может быть достаточно сильным, чтобы справиться со всеми повреждениями.
Это связано и с тем, что такое повреждение накапливается постепенно, его эффекты также проявляются не сразу. Например, они могут отражаться в постепенном увеличении смертности, начиная с раннего взросления [8]. Эти соображения подразумевают взаимную, кумулятивную причинную связь старения с участием всех процессов, даже если эти вклады сильно различаются как по форме, так и по влиянию. Но, вернемся к кожным процессам, хотя описывать их без связи со всем организмом - ненаучно и, как минимум, неверно.
Карбамилирование белков как один из факторов старения
Гликирование — не единственный тип неферментативной модификации долгоживущих молекул. Мы помним, что этот вариант плохой с точки зрения здоровья. По причине собственного продолжительного периода полураспада белки матрикса, такие как коллаген I типа (основная часть которого находится непосредственно в дерме) и эластин, являются предпочтительными мишенями карбамилирования.
Возникает резонный вопрос: “Как профилактировать, остановить и обратить вспять эти процессы?”
Согласно доступной информации проекты, наработки и перспективы у этого направления ведутся. Например: разработка комбинации ингибиторов КПГ (конечных продуктов гликирования). Такие комбинации могут включать:
- dPUFA (дейтерированные полиненасыщенные жирные кислоты) для уменьшения перекисного окисления липидов (дейтерированной линолевой, линоленовой, арахидоновой, эйкозапентаеновой или докозагексаеновой кислоты (около 20-25% для D2-Lin-PC и намного меньше для D10-DHA-PC (ReFresh). Показано соответствие между концентрациями дейтерированных фосфолипидов (ReLoad), эффективными для подавления перекисного окисления липидов, и концентрациями, обеспечивающими защиту целостности мембраны. Таким образом, продемонстрирован сильный защитный эффект небольших количеств D-ПНЖК в липосомальных бислоях);
- Соединения, содержащие О-ацетильную группу для защиты белков от гликирования за счет ацетилирования остатков лизина (интересный факт: утром этот процесс достигается быстрее, чем в вечернее время, а значит роль циркадных ритмов не упразднена);
- Соединения с трансгликирующей активностью: карнозин (о нем мы подробно поговорим ниже), ансерин;
- Амадорины для предотвращения превращения продуктов Амадори в КПГ;
- Генетическая модификация фибробластов.
Все это позволяет достичь целенаправленного удаления продуктов Амадори и оснований Шиффа, что перспективно предотвращает образование и накопление необратимых КПГ, таких как глюкосепан.
Интересный факт:
Всеми любимый витамин С - выступает патологическим фактором (может быть участником повреждений при возрастной катаракте и нейродегенеративных заболеваниях за счет вызываемого оксоальдегидного стресса). Кожный процесс отдельно не изучался, однако, четкую корреляцию проследить несложно [10]. Мы слышали с детства, как полезна аскорбиновая кислота, косметологи колют ее и капают в гипердозах чтобы помочь настимулировать коллаген, не зная базовых вещей о метаболизме межклеточного матрикса.
Краткая справка:
Оксоальдегидный стресс - это избыточное образование метилглиоксаля (предшественник КПГ (см.выше)) и его производного, КПГ под названием MG-H1.
Почему витамин С, являесь антиоксидантом, становится прооксидантом в этих органах? Все дело в ионах металлов (меди и железа): они являются основным механизмом перехода от антиоксидантной к прооксидантной роли аскорбиновой кислоты. Это подтверждается когортным исследованием с 25 тысячами шведских женщин, у которых добавки витамина С привели к увеличению образования катаракты после более чем 8-летнего наблюдения. Исследование подтверждает эту токсичность.
В заключении можно добавить, что именно аскорбиновая кислота, а не глюкоза, может быть основным источником гликированного повреждения при болезнях Альцгеймера и Паркинсона и катаракте.
И снова возвращаемся к непосредственно коже.
L-карнозин или бета-аланин-L-гистидин (ссылка на ReShape) способен разрушать основания Шиффа [2, 3]. Также одним из механизмов L-карнозина может быть его антифиброзное свойство у людей с сахарным диабетом, через ингибирование TGF-β [4, 5]. Это особенно актуально при возможных следствиях неэффективности косметологических процедур.
Правда, с 2015 года нам стало известно и о его положительной роли в комбинированной терапии (антигипертензивные препараты иАПФ, диуретики, БАБ и статины) при сердечной недостаточности. Первичный исход данного эксперимента - различия между двумя группами в эхокардиографических параметрах, в функциональной емкости и в оценке качества жизни через 6 месяцев после начала лечения, так как до начала эксперимента различий между двумя группами не было. В группе карнозина повысилась оценка качества жизни. [12]
Но, что более актуально сейчас, так это влияние карнозина на группы пациентов, где есть мутация филаггрина (структурный белок кожи, который специфически взаимодействует с промежуточными филаментами — кератинами), например, вульгарный ихтиоз, атопический дерматит, аллергическая сенсибилизация. Филаггрин содержит большое количество гистидина, который метаболизируется в транс-уроканиновую кислоту (транс-UCA) и пирролидон-5-карбоновую кислоту (РСА).
Ссылки на источники:
- Enzymatic deglycation with amadoriase enzymes from Aspergillus sp. as a potential strategy against the complications of diabetes and aging
- Carnosine and anserine act as effective transglycating agents in decomposition of aldose-derived Schiff bases
- Advanced glycoxidation and lipoxidation end products (AGEs and ALEs): an overview of their mechanisms of formation
- Carnosine as a protective factor in diabetic nephropathy: association with a leucine repeat of the carnosinase gene CNDP1
- L-carnosine inhibits high-glucose-mediated matrix accumulation in human mesangial cells by interfering with TGF-β production and signalling
- Stochastic non-enzymatic modification of long-lived macromolecules - A missing hallmark of aging
- A Tale of Two Concepts: Harmonizing the Free Radical and Antagonistic Pleiotropy Theories of Aging
- Aging: progressive decline in fitness due to the rising deleteriome adjusted by genetic, environmental, and stochastic processes
- Generation and Characterization of Anti-Glucosepane Antibodies Enabling Direct Detection of Glucosepane in Retinal Tissue
- Vitamin C is a source of oxoaldehyde and glycative stress in age‐related cataract and neurodegenerative diseases
- Vitamin C supplements and the risk of age-related cataract: a population-based prospective cohort study in women
- Effects of oral administration of orodispersible levo-carnosine on quality of life and exercise performance in patients with chronic heart failure
Предыдущий пост
Воспаление и старениеСледующий пост
Магний и его команда



